483简介
483是指美国食品药品监督管理局(FDA)发出的《观察记录表》(Form FDA 483),通常简称为“FDA 483”。
在FDA进行现场检查后,查员认为发现了对产品质量或合规性构成潜在风险的问题,他们会在检查结束时向受检单位发出FDA 483报告。这份报告列出了发现的问题、违规行为或不合规情况,要求受检单位采取纠正措施。FDA 483不代表违规、是一种警告,提示受检单位需要立即采取措施纠正问题,以确保产品的安全性、质量和符合法规。
483检查结果分为NAI、VAI、OAI三类,反映了FDA对企业合规性的评估结果。
分类一:NAI(No Action Indicated ),这一分类表示检查人员没有发现违规行为或重大问题,受检单位在本次检查中符合了FDA的要求,没有需要纠正的问题。
分类二:VAI(Voluntary Action Indicated),这一分类表示检查人员在现场检查中发现了一些问题或违规行为,但这些问题并不涉重大的合规性问题,需要采取自愿性的纠正措施。受检单位需要主动采取措施来解决这些问题,以符合FDA的要求。
分类三:OAI(Official Action Indicated),这一分类表示检查人员在现场检查中发现了严重的违规行为或合规性问题,需要采取正式的行政行动来加以解决。这可能包括警、产品召回、罚款、停产等措施,以确保受检单位在法规要求下进行有效纠正。
受检单位收到FDA 483后,通常需要向FDA提交一份书面回复,说明他们计划如何纠正发现的问题,并采取什么措施确保未来的合规性。FDA会对这些回复进行评估,并根据受检单位的反应和采取的措施决定是否需要进一步的监督、制裁或其他行动。
博普智库483查询工具-小程序
博普智库483工具汇集了FDA官方公布的483检查信息、483检查报告,并对公布的483检查信息做了可视化的图表分析。目前小程序提供了483报告查询工具。
在博普智库小程序底部菜单点击「法规」进入法规板块,再点击FDA-483报告。
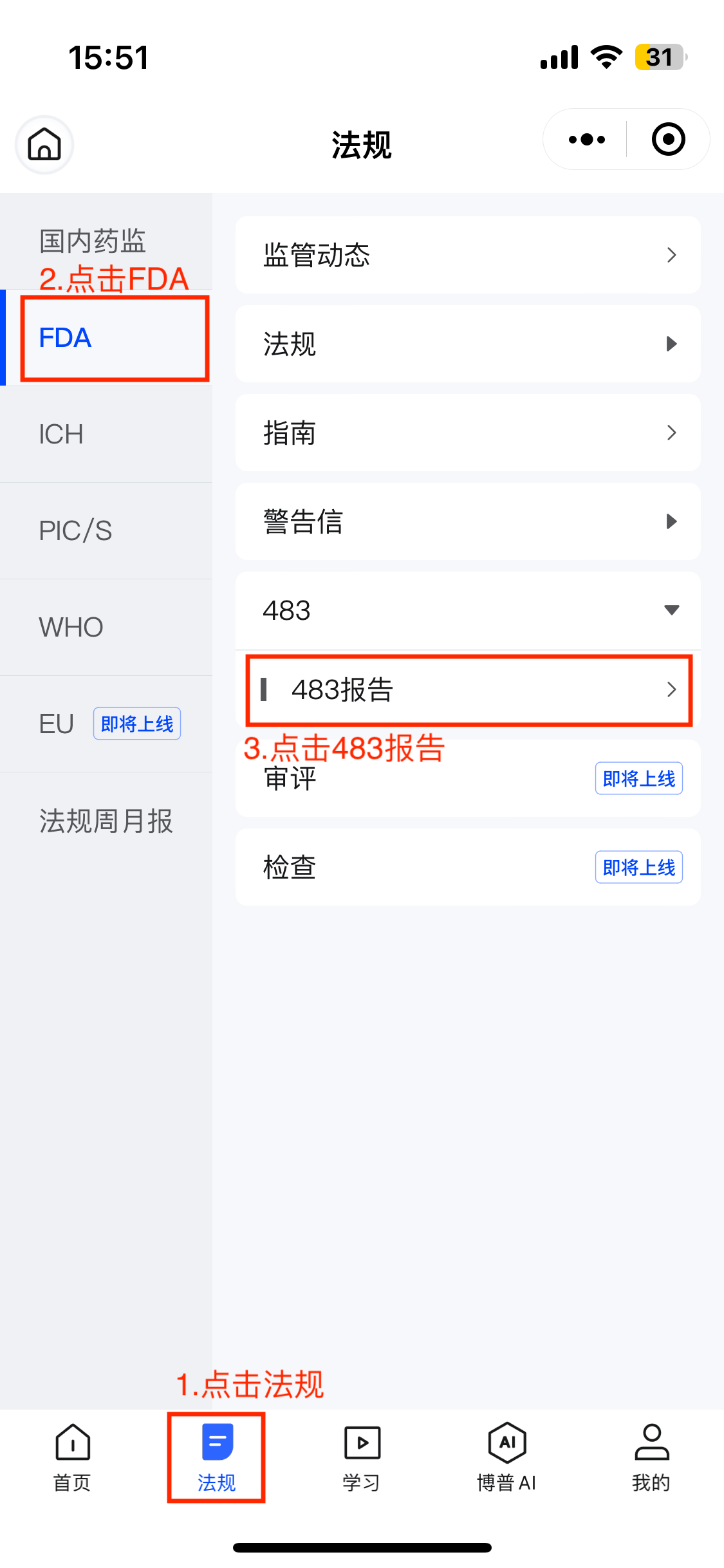
图1-483查询工具入口
在483报告列表可点击「名称」进入对应的报告详情。
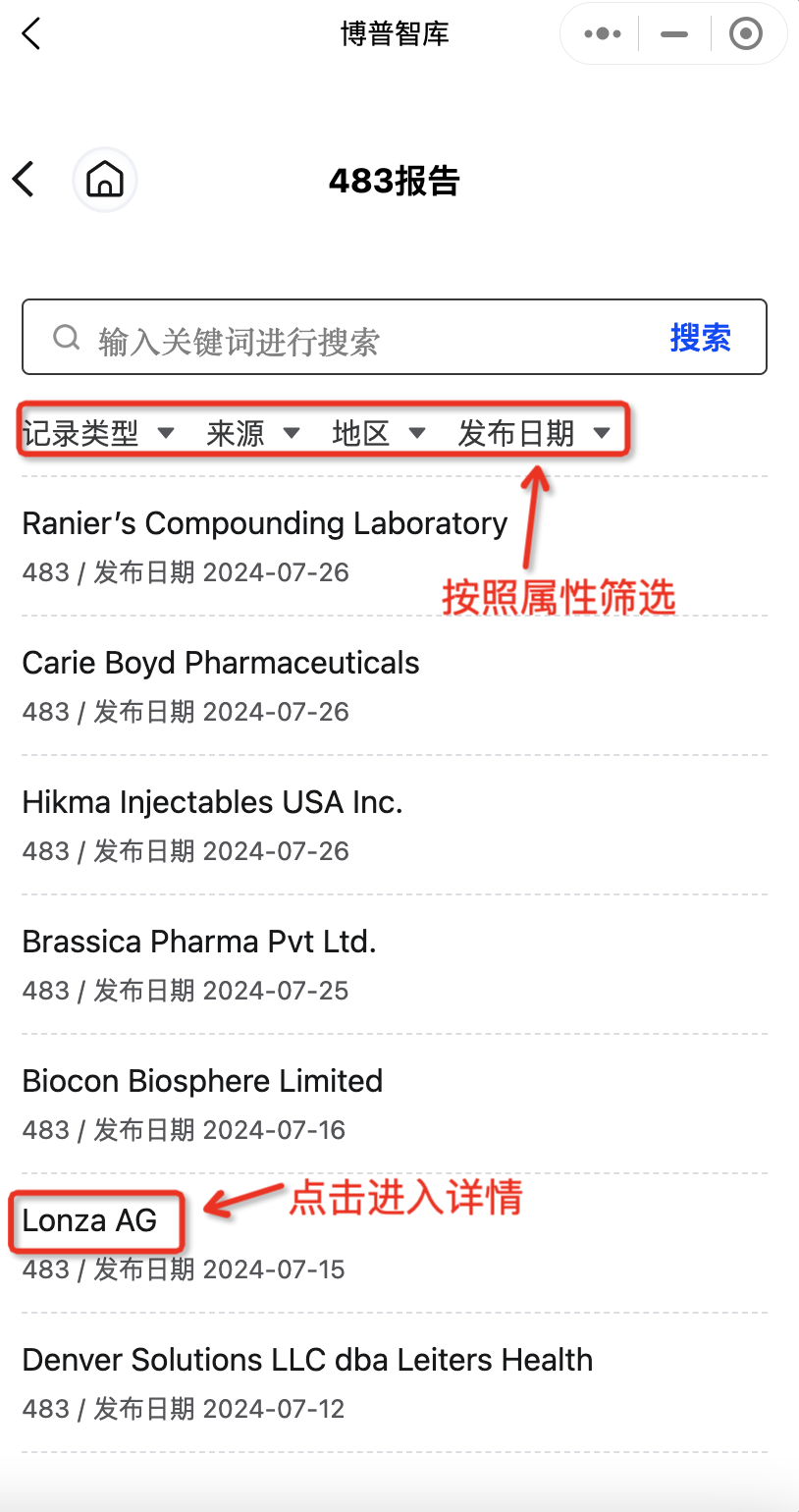
图2-483报告列表

图3-483报告详情

